ریزساختار آلیاژهای آهنی شامل فولادها و چدن ها می تواند از فازهای مختلفی تشکیل شده باشد. مهندسان متالورژی و سایر مهندسانی که در دوره کارشناسی دروسی از قبیل علم مواد را گذرانده اند، حداقل نامی از این فازها به گوششان خورده است. فریت، پرلیت، آستنیت، مارتنزیت، سمنتیت، گرافیت و بینیت، حتماً برای شمایی که با فولادها، چدن ها و بخصوص ریخته گری و عملیات حرارتی آن ها سر و کار دارید، نامی آشنا هستند.
ساختار کریستالی فلزات از کنار هم قرار گرفتن تعداد زیادی از سلول های واحد تشکیل یافته است. خود این سلول های واحد از آرایش منظم و تکرار شونده ی اتم های فلزی ساخته شده اند. در ساختار بلوری آهن، دو نوع سلول واحد وجود دارد. یک سلول واحد به شکل مکعبی است که اتم های آهن در مرکز و هر گوشه ی مکعب قرار گرفته اند (شکل ۱). سلول واحد دیگر به شکل مکعبی است که اتم های آهن در مرکز هر یک از وجوه مکعب و هر گوشه ی مکعب قرار گرفته اند (شکل ۲). به سلول واحد اول، شبکه مکعبی مرکز دار (body centered cubic) یا bcc و به سلول واحد دوم، شبکه مکعبی با وجوه مرکز پر (face centered cubic) یا fcc می گویند.
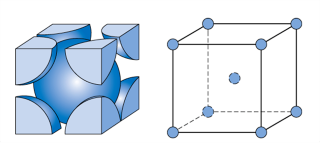
شکل ۱ – شبکه bcc
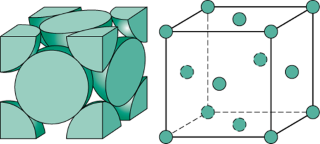
شکل ۲ – شبکه fcc
با شروع انجماد آهن در دمای ۱۵۳۸ درجه سانتیگراد، ساختار بلوری آهن جامد تا دمای حدود ۱۳۹۴ درجه سانتیگراد دارای شبکه کریستالی bcc است که به آن آهن دلتا (δ) می گویند. در این دما، ساختار آهن دچار تغییر شده و به شکل fcc در می آید که به آن آهن گاما (ϒ) می گویند. آهن گاما تا دمای حدود ۹۱۰ درجه سانتیگراد پایدار است. با عبور از این دما، ساختار کریستالی آهن باز تغییر یافته و دوباره شبکه bcc ظاهر می شود که به آن آهن آلفا (α) می گویند. آهن آلفا تا دمای محیط پایدار است. برای مشاهده ی دمای تشکیل و پایداری شبکه های بلوری مختلف آهن، نمودار تعادلی آهن-کربن (شکل ۳) را ببینید. با تغییر شبکه بلوری و نحوه ی آرایش اتم های آهن، خواص فیزیکی و مکانیکی آن نیز دچار تغییر می شود.
حتماً می دانید که فولاد آلیاژی از آهن بوده که از اضافه کردن کربن (از مقادیر بسیار جزئی تا ۲ درصد) به آن تشکیل می شود. کربن نقشی اساسی در فولادها دارد. حضور کربن باعث افزایش سختی، تنش تسلیم و استحکام کششی و کاهش درصد افزایش طول و مقاومت به ضربه فولادها و همچنین باعث سخت کاری یا آب دهی فولادها می شود.
کربن دارای چنان اتم های کوچکی است که وقتی به آهن اضافه می شود، می تواند بین اتم های آهن در شبکه های بلوری bcc و fcc قرار بگیرد و تشکیل یک محلول جامد را بدهد. محلول جامد فازی است که در آن اتم های یکی از عناصر آلیاژی می تواند در شبکه بلوری عنصر اصلی به صورت جانشینی (جایگزین یکی از اتم های عنصر اصلی) یا بین نشینی (در میان اتم های عنصر اصلی) قرار بگیرد. از آنجایی که آهن دارای سه نوع حالت کریستالی (آهن آلفا، گاما و دلتا) است، با قرارگیری کربن در بین اتم های این سه نوع آهن، سه نوع فاز (محلول جامد) در فولادهای ساده کربنی به وجود می آید که عبارتند از:
• فاز فریت (Ferrite) آلفا: محلول جامد بین نشین کربن در آهن آلفا با شبکه bcc (شکل ۴).
• فاز آستنیت (Austenite): محلول جامد بین نشین کربن در آهن گاما با شبکه fcc
• فاز فریت دلتا: محلول جامد بین نشین کربن در آهن دلتا با شبکه bcc
ناحیه ی تشکیل و حضور این فازها در فولاد ساده کربنی یا آلیاژ آهن-کربن را در دیاگرام زیر که به دیاگرام تعادلی آهن-کربن مشهور است، می توانید ببینید. میزان حلالیت یا درصد کربن بین نشین در هر یک از انواع آهن ها متفاوت است. در دیاگرام آهن-کربن، حداکثر میزان حلالیت کربن در آهن آلفا، گاما و دلتا به ترتیب ۰٫۰۲، ۲٫۱۱ و ۰٫۱ درصد نشان داده شده است. با توجه به دمای پایداری فریت دلتا (بیش از ۱۳۹۴ درجه سانتیگراد)، این فاز اهمیت زیادی در فولادهای کربنی ندارد، لذا منظور از فریت در مباحث بعدی، فریت آلفا است.
از آنجایی که بیشتر فولادها دارای عناصر آلیاژی به جز آهن و کربن هستند و این عناصر موقعیت مرز بین نواحی مختلف فازی و دما و گستره ی پایداری آن ها را نسبت به فولادهای ساده کربنی تغییر می دهند، دیاگرام آهن-کربن تنها به عنوان یک راهنمای عمومی استفاده می شود و کاربرد تخصصی در مطالعه ی فازی و عملیات حرارتی انواع فولادها را ندارد.
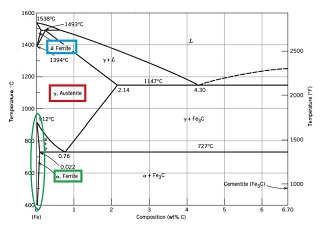
شکل ۳ – دیاگرام تعادلی آهن – کربن
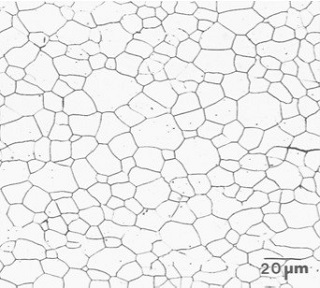
شکل ۴- دانه های فریت در فولاد کم کربن با ۰٫۰۲ درصد کربن – بزرگنمایی ۵۰۰
همان طور که اشاره شد، حلالیت کربن در آهن محدود می باشد. پس شاید این سوال پیش بیاید که چه بر سر کربن اضافی در ترکیب آلیاژ یا کربنی که نتوانسته در تشکیل محلول جامد بین نشینی کربن در آهن (فریت و آستنیت) شرکت کند، می آید؟
این کربن اضافی به دو صورت دیگر می تواند در آلیاژ آهن-کربن ظاهر شود:
۱- سمنتیت (Cementite) یا کاربید آهن (Iron Carbide): ترکیب بین فلزی سه اتم آهن و یک اتم کربن با فرمول Fe3C است که مقدار درصد کربن در آن، ۶٫۶۷ درصد است. شبکه بلوری سمنتیت از نوع bcc و fcc نیست، بلکه از نوعی شبکه بلوری دیگر به نام اورترومبیک است. سمنتیت یک فاز بسیار سخت و ترکیبی ناپایدار است.
۲- گرافیت (Graphite): اگر درصد کربن زیاد و سرعت سرد شدن آهسته باشد، کربن به صورت آزاد در ساختار باقی می ماند که به آن گرافیت می گویند. گرافیت در چدن ها (آلیاژهای آهن – کربن با بیشتر از ۲ درصد کربن) دیده می شود. ناپایداری سمنتیت باعث می شود که تحت شرایط خاص تجزیه شده و کربن آزاد یا گرافیت تولید کند.
با این توضیحات، تاکنون مشخص شده است که ساختار آلیاژهای فولاد کربنی در دمای محیط می تواند از محلول های جامد فریت و آستنیت و ترکیب بین فلزی سمنتیت یا کاربید آهن تشکیل شده باشد. علاوه بر این فازها، ساختارهای دیگری هم در فولادها دیده می شود که به صورت هیچ کدام از فازهای قبلی (محلول جامد بین نشین یا ترکیب بین فلزی) نیستند، بلکه از دگرگونی یا تغییر ساختار آستنیت به هنگام سرد شدن فولاد در عبور از دمای حدود ۷۲۷ درجه سانتیگراد به وجود می آیند. این فازها عبارتند از:
۱- پرلیت (Pearlite): پرلیت مخلوطی از لایه های متناوب دو فاز فریت و سمنتیت است که از دگرگونی آستنیت در هنگام سرد شدن آهسته و تحت مکانیسم نفوذ اتمی (جوانه زنی و رشد) به وجود می آید. شکل ظاهری پرلیت مشابه اثر انگشت بر روی کاغذ است.
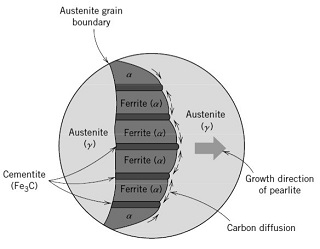
شکل ۵- شکل شماتیک تشکیل پرلیت

شکل ۶ – شکل ظاهری پرلیت، شبیه اثر انگشت
۲- مارتنزیت (Martensite): مارتنزیت یک فاز غیر تعادلی سخت است که از سریع سرد کردن آستنیت و طی یک استحاله غیر نفوذی تشکیل می شود. با تشکیل مارتنزیت، کربن محلول در شبکه bcc به مقدار زیادی افزایش یافته و جاهای خالی بیشتری از شبکه توسط کربن اشغال می شود. در نتیجه، شبکه بلوری از bcc مکعبی به bct مکعب مستطیلی تغییر می یابد.

شکل۷ – شکل ظاهری مارتنزیت در ساختار فولاد
۳- بینیت (Bainite): بینیت یک فاز غیر تعادلی سخت است که از سریع سرد کردن آستنیت (مثل مارتنزیت) ولی طی یک استحاله نفوذی (مثل پرلیت) تشکیل می شود. بینیت مثل پرلیت مخلوطی از فازهای فریت و سمنتیت است، با این تفاوت که فریت و سمنتیت به صورت لایه های متناوب کنار هم قرار نگرفته اند، بلکه در این ساختار، صفحات فریتی، ذرات سمنتیتی را در بر گرفته اند (بینیت پایینی) یا اینکه ذرات سمنتیت در فصل مشترک فریت – آستنیت و بین صفحات فریتی جوانه زده و رشد می کند (بینیت بالایی). بینیت مثل مارتنزیت به صورت سوزنی شکل دیده می شود.
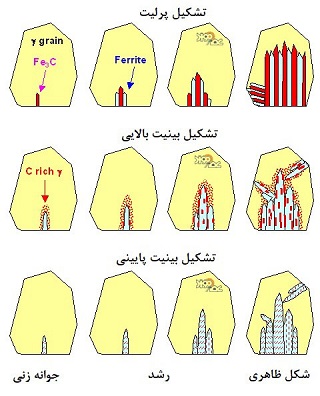
شکل ۸ – مورفولوژی جوانه زنی و رشد پرلیت و بینیت
منبع: عصر مواد